美国取消数十家厂家EUA授权,EUA申请条件发生重大变化
文章来源:FDAI 录入:深圳华道顾问 添加时间:2020/5/8
5月7日,美国FDA针对“未能符合NIOSH标准的产自中国的一次性过滤口罩(FFR)”修改了原先的 EUA(紧急使用授权)政策,同时更新了EUA 中国口罩生产商的授权列表(附录A https://www.fda.gov/media/136663/download),将数十家中国生产商从EUA口罩授权列表上撤除。原因是,NIOSH对列表上的过滤式口罩进行抽样检测时,它们的过滤能力受到质疑,某些抽样口罩的过滤能力未能达到最低95%过滤效率的要求。
EUA的申请条件发生重大变化
根据我们先前发布的文章,2020年4月3日,美国FDA 扩大了EUA 授权的申请范围,专门为中国生产的未经NIOSH批准的过滤式口罩(即KN95)开设了EUA申请通道。当时,FDA针对中国生产商发布了三项申请条件。不过现在,这些原先的申请条件已经发生了重大变化。
根据FDA最新的规定,中国生产的未经NIOSH批准的过滤式口罩想要申请EUA授权出口美国,必须符合以下任一条件:
1. 持有其他型号过滤口罩一个或多个NIOSH 许可。
2. 持有相应的省级或市级监管机构颁发的中国国家药品监督管理局(NMPA)的注册认证,并得到美国FDA的核实和验证。
3. 之前曾被列上 附录 A(EUA授权列表)名单上的中国生产商,请在自5月7日起45天内提交NIOSH标准测试程序TEBAPR-STP-0059的测试结果,最大或最小过滤效率要达到或高过95%。
FDA还规定,今后只允许生产商提交EUA申请,不再接受美国进口商的申请。另外,已经列上授权列表(附录 A )的过滤口罩若未能符合其中某项申请标准的话,将会被FDA从授权列表上撤下来。
以下是目前为止仍列在EUA列表中的14家中国生产商名单:
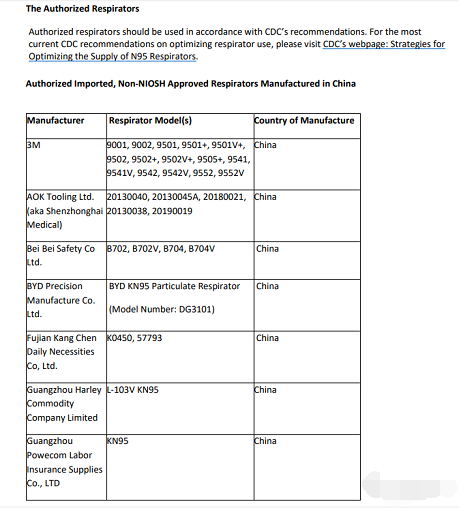
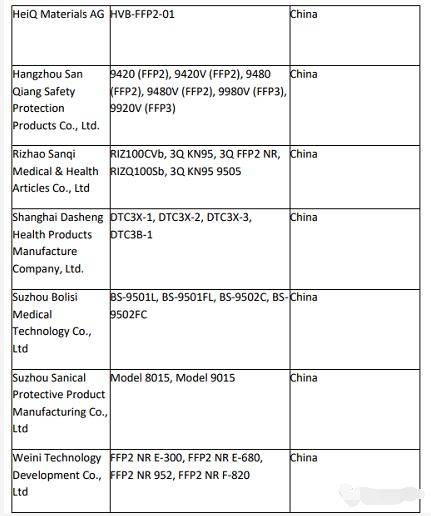
(数据来源:美国FDA网站)
被移除EUA列表(附录 A)的口罩生产商
那些曾根据 “生产商或进口商所提交的公认独立实验室检测报告”而获得EUA授权的口罩生产商,FDA修改了它们的EUA授权资格,现已经将所有基于该条件而获得授权的过滤口罩从附录 A 上撤除。不过,那些未能符合特定性能标准的过滤口罩,若重新达到最新的EUA申请条件,那可以申请重新列上授权列表(附录 A)。
我们在网站上专门开设了COVID-19贸易资源页面(https://benjaminlengland.com/problems-we-solve/covid-19-resources-for-life-sciences-and-other-goods/),上面集中了疫情期间美国FDA和中美关税所有最新的法规和政策动态,您可以通过访问链接获取所需要的资源和信息。我们的监管顾问和律师可帮助生产商申请EUA。
【相关文章】

 当前位置:
当前位置: